治療薬開発に、患者と家族も協力を
病気のメカニズムに基づく根本治療薬
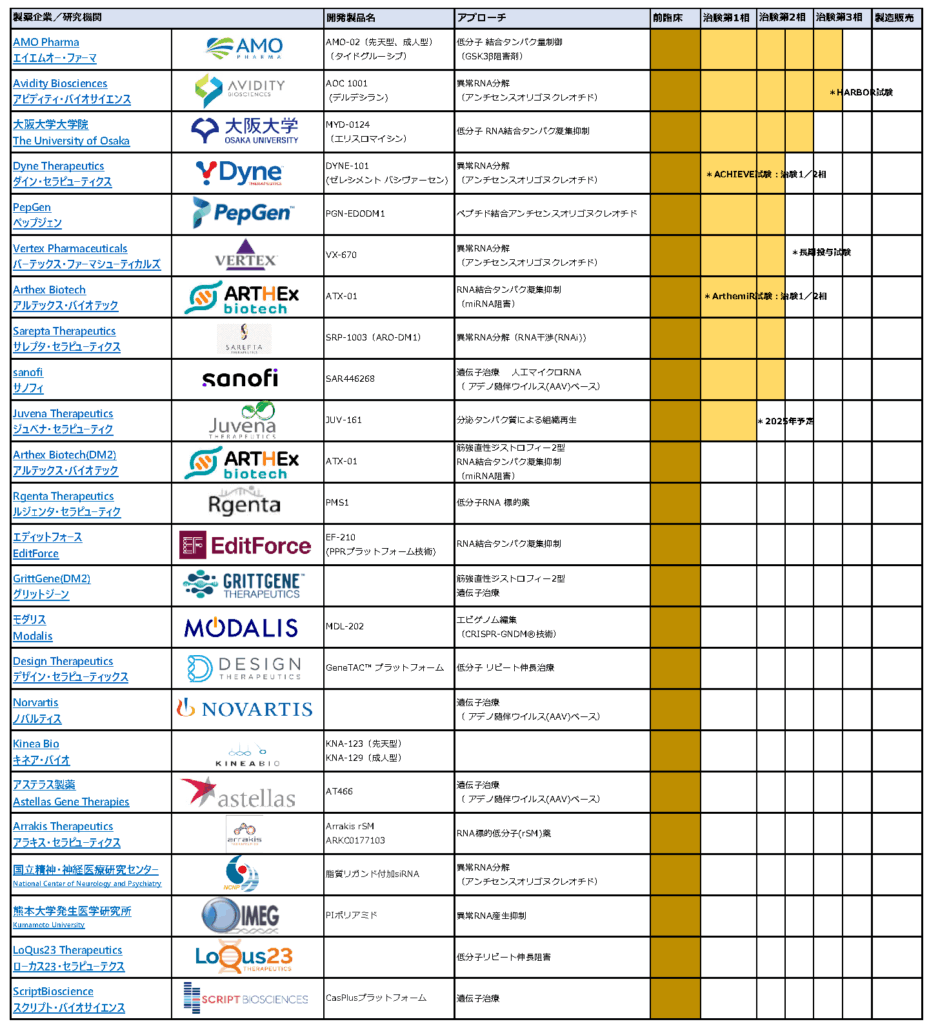
2025年11月16日、筋強直性ジストロフィー患者会(DM-Family)では、筋強直性ジストロフィーで現在進んでいる治療薬開発一覧表をアップデートしました。今回から、日本の患者・家族にもわかりやすく、企業名をカタカナで記載しました。
治験実施中の研究をはじめ、アメリカ食品医薬品局(FDA)に新薬候補臨床試験の開始届(IND:Investigational New Drug)を提出・承認を待つ研究、非臨床の研究など、海外・日本国内を含め多くの製薬企業、研究者が競って筋強直性ジストロフィー治療薬の開発を進めています。
![]() PDFはこちらです。(上記の表をクリックしてもPDFをご覧いただけます)
PDFはこちらです。(上記の表をクリックしてもPDFをご覧いただけます)
日本でも治療薬を!
日本で処方される医薬品は、独立行政法人 医薬品医療機器総合機構(PMDA)で承認される必要があり、そのためには国内で治験を行って安全性と有効性を確認します。
海外で開発中の治療薬について、日本でも治験を実施するためには、さまざまな困難があります。
治験には莫大な費用がかかるうえ、言葉や文化が異なる海外の製薬企業にとって、日本での実施は大きな負担となります。
それでも、日本でも治験をしようと思ってもらうためには、患者自身が力を合わせて、次のことを行う必要があります。
- 遺伝子検査により、筋強直性ジストロフィーであることを確定させたうえで患者登録を行い、治験ができる患者がそろっていることを海外製薬企業や研究機関などにも示していく。
- 自然歴研究※に参加し、治験の基礎となるデータを提供する。
※自然歴研究については下記を参照ください。
治療法開発に貢献できる。研究班「自然歴研究」参加者募集
患者も家族も、みんなで協力し合って治療薬を手にしませんか。
合併症に向けた対症療法薬
筋強直性ジストロフィーの筋強直(ミオトニア)や日中過眠、インスリン抵抗性に向けた治療薬も、海外では治験が進んでいます。
日本でもこうした薬を使うためには、有効性や安全性について確かなデータや科学的根拠を示し、承認を受けることが必要です。
承認されていない薬を処方することは「適応外処方」となり、原則として認められません。
ミオトニアを緩和する「メキシレチン」は、不整脈を起こすリスクが国内外の診療ガイドラインでも示されています。ウオームアップで緩和するなど、患者自身の方法を見つけていくことをお勧めします。